NK细胞实验Protocol
NK细胞又称为自然杀伤细胞,属于大颗粒淋巴细胞,来源于骨髓,占外周血淋巴细胞的5%~15%,是重要的免疫细胞。科学家在1975年首次鉴定到了NK细胞,这类细胞能够在缺少T、B细胞的情况下直接杀伤肿瘤细胞。与具有细胞毒性的CD8+ T细胞不同,NK细胞杀伤肿瘤细胞时不需要预先致敏可以直接杀伤MHC阴性的肿瘤细胞,这使得NK细胞在过继细胞免疫治疗中被广泛应用。但NK细胞在外周血淋巴细胞中所占的比例相对较低,所以有必要对种NK细胞进行体外扩增,用于研究NK细胞的功能并为细胞免疫治疗提供支持。
NK细胞的分离和纯化
从外周血中获得PBMC
要从外周血中获得NK细胞,第一步是将外周血中大部分的红细胞和粒细胞去掉,获得外周血单个核细胞(PBMC)。最常规的方法是利用密度梯度离心法获得PBMC,这里小编向您安利一种能够轻松、快速获得PBMC的神器―SepMate离心管(# 86415)(感兴趣的盆友可以来和我们咨询申请试用)。具体步骤如下:
使用Sepmate专用的密度梯度离心管。确保样本、含2%胎牛血清(FBS)的PBS缓冲液(PBS+2% FBS)、密度为1.077±0.001的密度梯度离心液,如(Lymphoprep,#07851)以及离心机均处于室温(15 - 25°C)。
1、将密度梯度离心液通过SepMate密度梯度离心管隔板中央小孔小心加入SepMate密度梯度离心管中。加入体积请参考下表。密度梯度离心液的液面应淹没过隔板,如果在离心液在隔板下有一些小气泡,不必担心,这些气泡不会对使用效果产生影响。
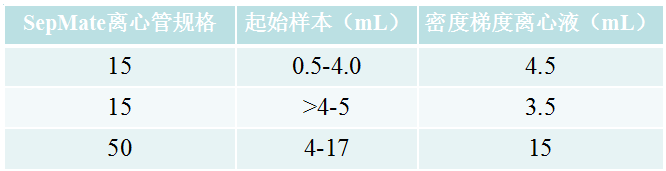
2、使用等体积的PBS+2%FBS稀释血液样本并将其混匀。
3、保持SepMate密度梯度离心管垂直,用移液器沿管壁加入稀释后的样本。样本将会在隔板上面与密度梯度离心液混合。
4、在室温下1200 x g,离心10分钟,无需调慢离心机降速。
注意:对于存放超过24小时的样本,建议离心时间为20分钟。
友情提示:
g与RPM的换算公式如下:


RPM = 离心机的转速,以每分钟转数计算
RCF = 相对离心力(g)
Radius = 离心机转子的半径,用厘米(cm)表示
5、倒出上层液体至一个新的离心管,该层含富集的PBMC。请勿将SepMate密度梯度离心管在倒置状态下超过2秒。
注意:离心后可能会有少量红细胞(RBCs)出现在SepMate隔板的表层,这些RBCs不会对使用效果产生影响。为减少富集MNCs中的血小板污染,在倾倒前可用移液管吸去MNC层上方的一些上清液。
6、使用PBS + 2% FBS清洗PBMC两次。
注意:
① 清洗细胞时建议在室温下300 x g离心8分钟,无需调慢离心机降速。如果血样中血小板含量较高,可在第二次清洗时以120 x g离心10分钟(将离心机降速调慢),可有效减少血小板的污染。
② 如果离心后隔板上的密度梯度离心液出现红色(即部分红细胞没有沉降),可以将SepMate离心管再以1200 xg 离心10 分钟,无需调慢离心机降速。在处理存放超过24 小时的样本时可能需要这一步骤。
从PBMC中富集NK细胞
利用NK细胞磁珠分选试剂盒将NK细胞(# 17955)从PBMC中富集获得(厉害了,word天!该磁珠分选试剂盒的分选流程非常简单快速,所有步骤仅需8分钟!)
1、将PBMC计数,并将细胞浓度调至5x10^7/mL,将细胞加入流式管中(Corning # 352058)。
2、加入抗体混合物,50μL/mL PBMC样本,充分混匀,室温下孵育5分钟。
3、用涡旋器充分震荡涡旋磁珠RapidSpheres30秒钟。
4、将磁珠以50μL/mL PBMC加入样本,充分混悬后立刻进行下一步,无需孵育!
5、加入缓冲液(DPBS+2%FBS+1mmEDTA)至终体积2.5mL,充分混悬。
6、将流式管插入配套磁极(# 18000),室温下静置3分钟。
7、拿起磁极,动作连贯地倒置磁极和试管,将未经标记的细胞倒入另一个干净的试管。将磁极和试管导致状态下保持2-3秒后恢复正立状态,请勿摇晃试管口或接触可能挂在管口的液滴。
注意:偶尔会发生NK细胞纯化所得细胞过少的情况,这主要是样本的差异性所致,有些供者的血样其NK细胞本身含量过低。(因此最好每次都保留少量分选前样本,对其进行NK细胞含量的检测,如果NK细胞分选得率过低,可以排除是因为样本原因还是操作问题)。
扩增NK细胞
在对NK细胞进行扩增中,人们先是通过单独添加大剂量IL-2,实现了一些NK细胞的扩增(培养时间超过1-2周,扩增5-10倍)。另外,通过激活自体T细胞介导NK细胞的扩增,大概也是通过释放了部分细胞因子。因此人们通过利用间质基质细胞或人工抗原呈递细胞(aAPC)支持来源于外周血和脐带血的NK细胞的扩增。被应用较多的是用4-1BBL(CD137L)和膜结合IL-15(mIL-15)7转导的基于K562的aAPC,其在21天内实现了NK细胞平均扩增277倍。虽然使用K562-41BBL-mIL15 aAPC扩增的NK细胞在体外和体内与未扩增的NK细胞相比具有高度细胞毒性,并且参与抗体依赖的细胞介导的细胞毒性(antibody-dependent cell-mediated cytotoxicity,ADCC),但是它们的增殖受到归因于端粒缩短的衰老的限制。最近报道使用K562表达MICA,4-1BBL和IL159的NK细胞的350倍扩增。为进一步完善NK细胞的制备技术和促进其在临床应用奠定基础。
下面介绍的就是应用较多的利用K562细胞做为饲育层细胞扩增细胞的方法
扩增NK细胞的方式有两种,一种是直接从PBMC中扩增,另一种是对已经纯化的NK细胞进行扩增。
注意:直接对PBMC进行扩增,NK细胞的扩增率取决于PBMC中NK细胞的含量,因此可能存在样本差异性。
扩增流程 - 第一阶段刺激
1、第0天
对于扩增5x106PBMC,计数1x107的K562 Cl9 mIL21细胞并用伽马射线100Gy照射。
2、照射后,用PBS洗涤细胞并用NK扩增培养基(NKEM)重悬细胞。
NK扩增培养基的配制

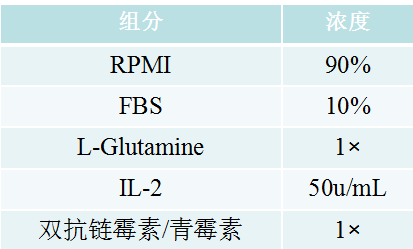
3、将PBMC(5x106)和照射后的K562 Cl9 mIL21(1x107)以1:2比例接种于40mLNKEM中,将40mL NKEM混悬的细胞混合物接种于T75培养瓶中,然后直立置于37℃,5%CO2培养箱中孵育。
4、第3天和第5天
400x g离心5分钟收集细胞,用新鲜的NKEM进行半换液(在整个培养基体积中加入新鲜的IL-2)继续共培养。
扩增流程 - 第二阶段刺激
1、第7天
在第一星期末进行细胞计数。
2、用5x105细胞进行流式检测细胞表型:经常使用CD56-FITC、CD16-PE和CD3-PE-cy5进行表型检测,CD3-/CD16-/CD56+细胞为NK细胞。
3、对每5x106细胞进行再次刺激,计数1x107 K562 Cl9 mIL21细胞并用伽马射线100Gy照射。
4、加入等量照射过的K562 Cl9 mIL21(比例1:1),用NKEM重悬至2.5x105 细胞/ mL。
注意:每次更换培养基或刺激,重悬细胞至2.5 x 105细胞/mL,在扩增的最高峰阶段,每毫升PBMC/NK细胞数量也要不高于2.0 x 106 以防止营养物质的过度消耗,有助于实现最大的扩增效率,且提高细胞存活率。
5、将细胞接种于T75培养瓶(每个培养皿瓶中最多接种50mL,即最多1.25x107细胞)。然后直立置于37℃,5%CO2培养箱中。
6、第10天和第12天
对细胞计数。
7、根据细胞量更换所有培养基。并将细胞重悬至2.5x105 细胞/ mL,将细胞接种于T75培养瓶(每个培养皿瓶中最多接种50mL,即最多1.25x107细胞)。然后直立置于37℃,5%CO2培养箱中。
8、第14天
在扩增的第14天,计数培养的细胞。
9、用5x105细胞进行流式检测细胞表型(同第2步)。
10、如果是使用的PBMC进行的扩增,那么NK细胞在扩增阶段得以被纯化。如果扩增开始于纯化的NK细胞,直接进行第三阶段刺激。
11、纯化后,用5x105细胞进行流式检测,确定NK细胞的纯度。
12、使用所有纯化的NK细胞进行第三阶段刺激。
注意:NK细胞的扩张率依赖于样本的情况。在第1、2阶段的刺激结束时,所纯化得到的NK细胞可以被冻存。也可以根据实验需要用其中的一部分细胞再次刺激进行扩增。
扩增流程 - 第三阶段刺激
1、对细胞进行计数,根据细胞量,以1:1比例重悬NK细胞和照射过的 K562 Cl9 mIL21细胞(注意事项同第4步)。
2、第17天和第19天
对细胞进行计数。
3、根据细胞数量更换新鲜的NKEM培养基。
4、第21天
扩增到第21天,对扩增的细胞进行计数。
5、用1x106细胞进行流式分析,检测NK细胞表型。
6、FBS+10%DMSO冻存细胞,每管冻存5x107 细胞以备将来使用。
NK细胞毒性检测
1、毒性检测前一天,复苏1管已经冻存的或扩增的NK细胞并接种在NKEM中。
2、对于每个细胞毒性检测试验,使用一种靶细胞系,需要6x105NK细胞和3x105靶细胞。
注意:为了减少误差,建议使用至少7x105个NK细胞重新悬浮在700ul NKEM中,4x105 Calcein-AM染色的靶细胞重新悬浮于4mL NKEM中,用于细胞毒性测定实验。如果使用多通道移液管接种靶细胞,则可能需要基于所使用的培养器皿的大小,更多体积量的细胞(最多6×105细胞溶于6mL NKEM中)。另外,推荐的NK细胞数是专门针对方案中显示的E:T比例,如果使用较高的E:T比值相应增加NK细胞数(例如,对于40:1 E:T比使用4x106个细胞/mL)。
3、通过用NKEM稀释Calcein-AM(以1 mg/mL母液储存于DMSO中)制备CAM培养基。建议使用1:500,1:400,1:300, 1:200和1:100的稀释度对Calcein-AM进行稀释滴定,以达到最优浓度,使荧光效果最佳。
4、用1 mL CAM培养基重悬1 x 106靶细胞。37℃,孵育1小时,期间时常对细胞进行晃动。
注意:Calcein AM 是一种可以透过细胞膜的活细胞标记染料。进入细胞后,细胞内酯酶会切断乙酰羟甲基酯 (AM) 的酯基,产生无法透过细胞膜的 Calcein 荧光染料。凋亡细胞和死细胞的细胞膜已被破坏,无法保留 Calcein。Calcein 的最佳激发波长为 495 nm,发射波长为 515 nm。
5、重悬NK细胞至1x106细胞/mL,然后在圆底96孔板每三孔添加200 μL NK细胞悬液,使E:T(效应细胞:靶细胞)比例10:1相符合。
6、除达到最大体积的培养孔,在其它所有剩余的培养孔中添加100uL完全培养基。
7、在最大体积培养孔中加入100uL 2% Triton X-100。
8、通过每次转移100uL细胞,进行NK细胞梯度稀释,从而达到5个梯度的E:T比例。混匀。从最后一个培养孔中去掉100uL(E:T为0.3125:1)。
9、Calcein标记1小时候后,用NKEM培养基洗涤靶细胞两次,1200rpm离心5分钟。
注意:如果进行ADCC实验,在加Calcein标记45分钟后,加入10μg诱导靶细胞ADCC的特异性抗体。15分钟以后,在完全培养基中洗涤两次靶细胞,以1200rpm离心5分钟。以1×10 5个细胞/ mL重悬细胞并继续进行的下一步骤。
10、再次计数靶细胞,并重悬至1x105 细胞/mL。
11、每孔中加入100μL(1x104细胞/孔)靶细胞。100 x g离心1分钟开始细胞接触。
12、37℃,5% CO2条件下孵育4小时。
13、用100uL移液管轻轻混匀培养物,混匀悬浮释放的calcein,100 x g慢速离心培养板5分钟使细胞成团并将100uL上清液小心转移至新的培养板,避免产生气泡。如果有气泡可以用针将气泡刺破。
14、采用荧光读板器读板(激发滤光片485 nm,发射滤光片530 nm)。最大体积培养孔中得到最大释放量,其余培养孔获得测试释放量。
15、根据公式[(测试释放量-自发释放量)/(最大释放量-自发释放量)x 100计算百分比特异性裂解。


